Asam Amino: Struktur, Klasifikasi, dan Perannya dalam Metabolisme & Kesehatan
Asam amino adalah senyawa organik esensial yang berperan sebagai blok penyusun utama protein dalam semua makhluk hidup. Dengan struktur dasar yang terdiri dari gugus amina (-NH₂), gugus karboksil (-COOH), atom hidrogen, dan rantai samping (R-group), asam amino memiliki karakteristik unik yang menentukan sifat dan fungsinya dalam tubuh. Selain berperan dalam sintesis protein, asam amino juga berpartisipasi dalam metabolisme energi, sintesis neurotransmitter dan hormon, regulasi pH, serta proses detoksifikasi. Terdapat 20 jenis asam amino standar yang diklasifikasikan berdasarkan sifat kimia, kebutuhan nutrisi, dan peran biologisnya. Keberadaan dan keseimbangan asam amino dalam tubuh sangat penting untuk pertumbuhan, perkembangan, serta fungsi seluler yang optimal, menjadikannya komponen krusial dalam bidang biokimia, nutrisi, dan kedokteran.
1. Definisi, Struktur dan Komponen Asam Amino
1. Definisi Asam Amino
Asam amino adalah molekul organik yang berfungsi sebagai penyusun utama protein dalam semua bentuk kehidupan. Secara kimia, asam amino terdiri dari satu gugus amina (-NH₂), satu gugus karboksil (-COOH), atom hidrogen, dan rantai samping (R-group) yang berbeda-beda, yang menentukan sifat unik setiap asam amino.
Sebagai monomer protein, asam amino berperan dalam berbagai fungsi biologis seperti sintesis enzim, hormon, neurotransmitter, dan sebagai sumber energi dalam kondisi tertentu. Di dalam tubuh, asam amino dapat berasal dari makanan (esensial) atau diproduksi sendiri (non-esensial).
2. Struktur Dasar Asam Amino
Setiap asam amino memiliki struktur dasar yang sama, terdiri dari:
A. Komponen Utama Asam Amino
- Gugus Amina (-NH₂) → Bersifat basa, dapat menerima proton (H⁺) dalam larutan.
- Gugus Karboksil (-COOH) → Bersifat asam, dapat melepaskan proton (H⁺).
- Atom Karbon Alfa (Cα) → Pusat utama yang menghubungkan semua gugus.
- Rantai Samping (R-group) → Struktur yang berbeda untuk setiap asam amino, menentukan sifatnya (polar, nonpolar, asam, atau basa).
- Atom Hidrogen (-H) → Terikat langsung ke karbon alfa.
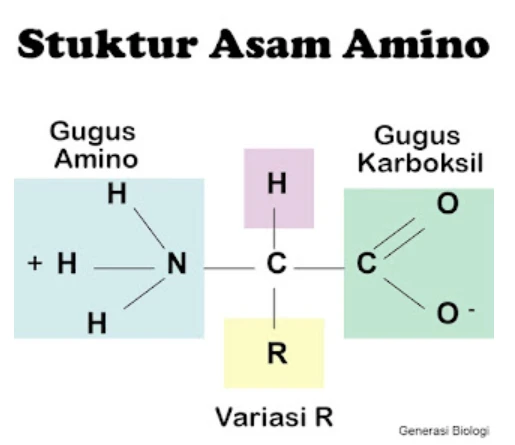
B. Rumus Umum Asam Amino
H2N−CH(R)−COOHH_2N - CH(R) - COOHH2N−CH(R)−COOH
Di mana:
- NH₂ = Gugus amina.
- COOH = Gugus karboksil.
- R = Rantai samping yang unik untuk setiap asam amino.
Contoh Struktur Asam Amino (Glisin)
H_2N - CH_2 - COOH ]
(Glisin memiliki R-group = Hidrogen)
C. Bentuk Isomer Asam Amino
Asam amino (kecuali glisin) memiliki pusat kiral, yaitu atom karbon yang terikat pada empat gugus berbeda, sehingga menghasilkan dua bentuk isomer:
- L-Asam Amino → Digunakan dalam sintesis protein biologis.
- D-Asam Amino → Jarang ditemukan dalam sistem biologis, lebih sering ditemukan dalam dinding sel bakteri.
3. Komponen Penyusun Asam Amino
Asam amino tersusun dari unsur dasar yang membentuk komponen molekulnya:
A. Unsur Kimia Penyusun
- Karbon (C)
- Hidrogen (H)
- Oksigen (O)
- Nitrogen (N)
- Sulfur (S) (hanya dalam asam amino tertentu seperti metionin dan sistein)
B. Rantai Samping (R-Group)
Rantai samping inilah yang menentukan sifat unik dari masing-masing asam amino. Berdasarkan sifat kimia rantai sampingnya, asam amino dapat dikategorikan sebagai:
- Nonpolar (Hidrofobik) → Tidak larut dalam air (contoh: alanin, valin, leusin).
- Polar Tidak Bermuatan → Larut dalam air, tetapi tidak membawa muatan (contoh: serin, treonin).
- Bermuatan Positif (Basa) → Mengandung gugus yang bersifat basa (contoh: lisin, arginin).
- Bermuatan Negatif (Asam) → Mengandung gugus karboksil tambahan (contoh: aspartat, glutamat).
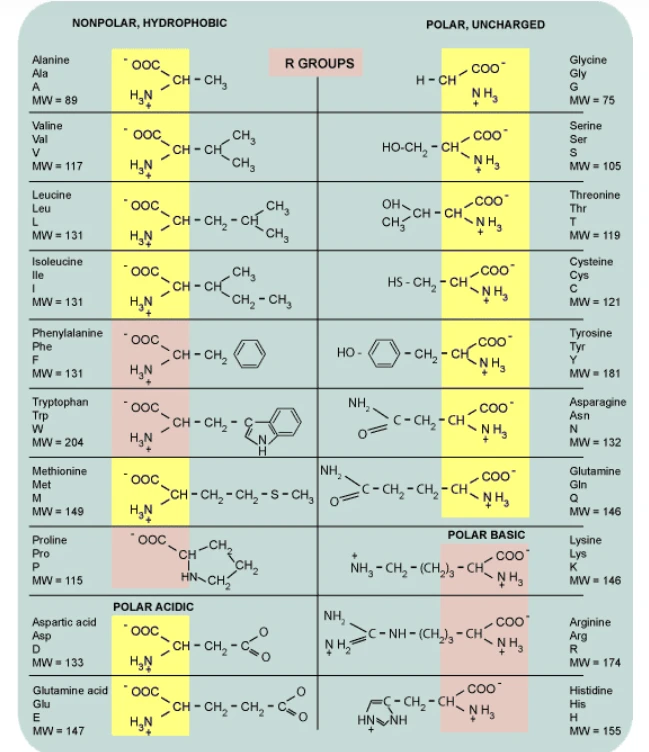
C. Kelompok Fungsi dalam Asam Amino
Selain gugus amina dan karboksil, beberapa asam amino memiliki gugus tambahan seperti:
- Hidroksil (-OH) dalam serin dan tirosin.
- Sulfhidril (-SH) dalam sistein.
- Amina tambahan (-NH₂ atau =NH) dalam lisin dan arginin.
- Gugus aromatik dalam fenilalanin dan triptofan.
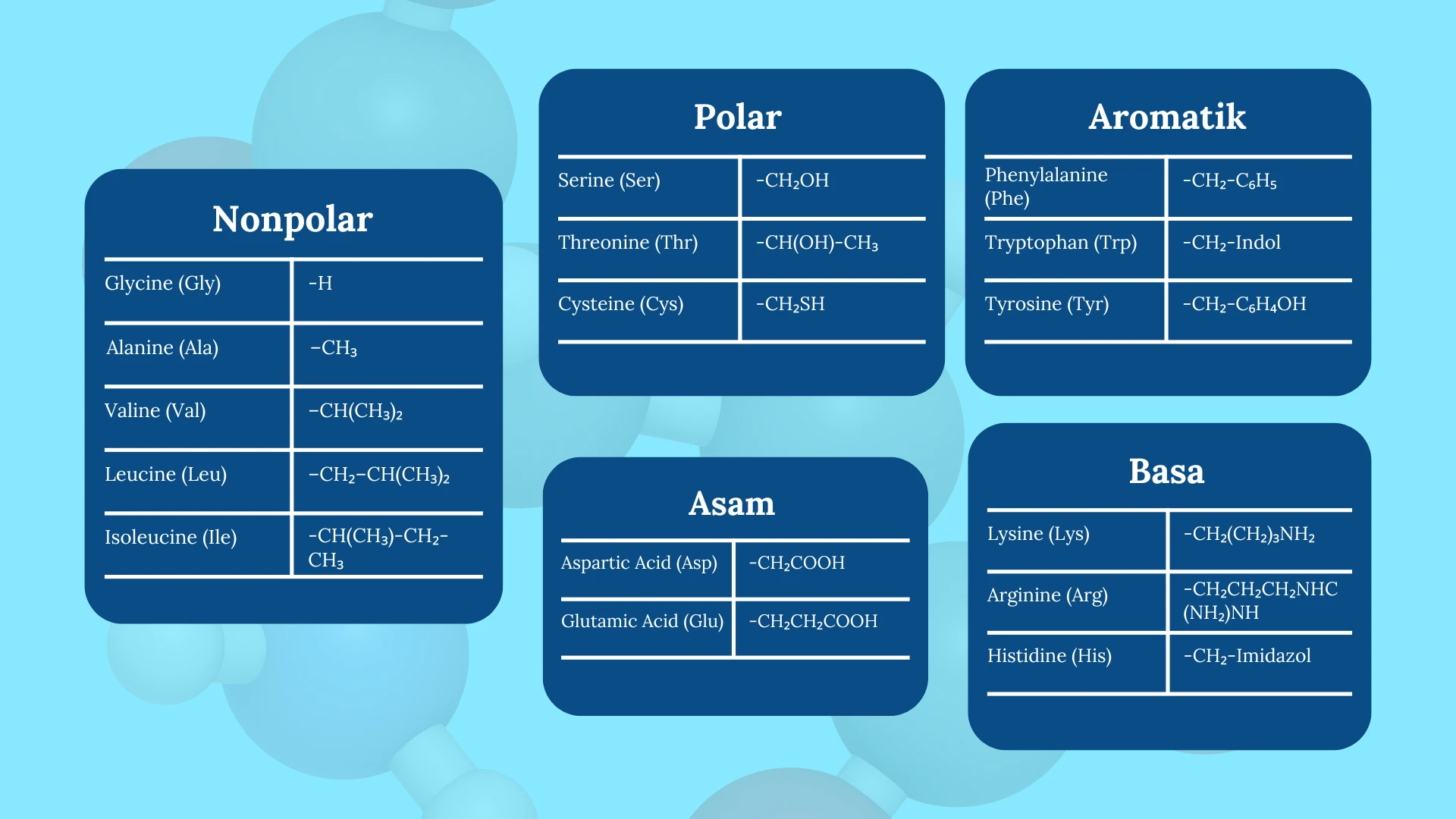
2.Klasifikasi Asam Amino
A. Berdasarkan Sifat Kimia Rantai Samping
Asam amino diklasifikasikan berdasarkan sifat rantai samping (R-group), yang menentukan bagaimana mereka berinteraksi dengan air, lipid, dan molekul biologis lainnya. Sifat kimia ini sangat penting dalam menentukan struktur dan fungsi protein.
Terdapat empat kategori utama berdasarkan sifat kimia rantai sampingnya:
- Asam Amino Nonpolar (Hidrofobik)
Asam amino dalam kelompok ini memiliki rantai samping yang bersifat nonpolar dan tidak larut dalam air. Mereka sering ditemukan di bagian dalam protein globular, karena interaksi hidrofobik yang membantu menjaga struktur protein.
Ciri-ciri:
- Tidak larut dalam air.
- Rantai samping terutama mengandung karbon dan hidrogen.
Cenderung berlokasi di inti protein globular (jauh dari air).

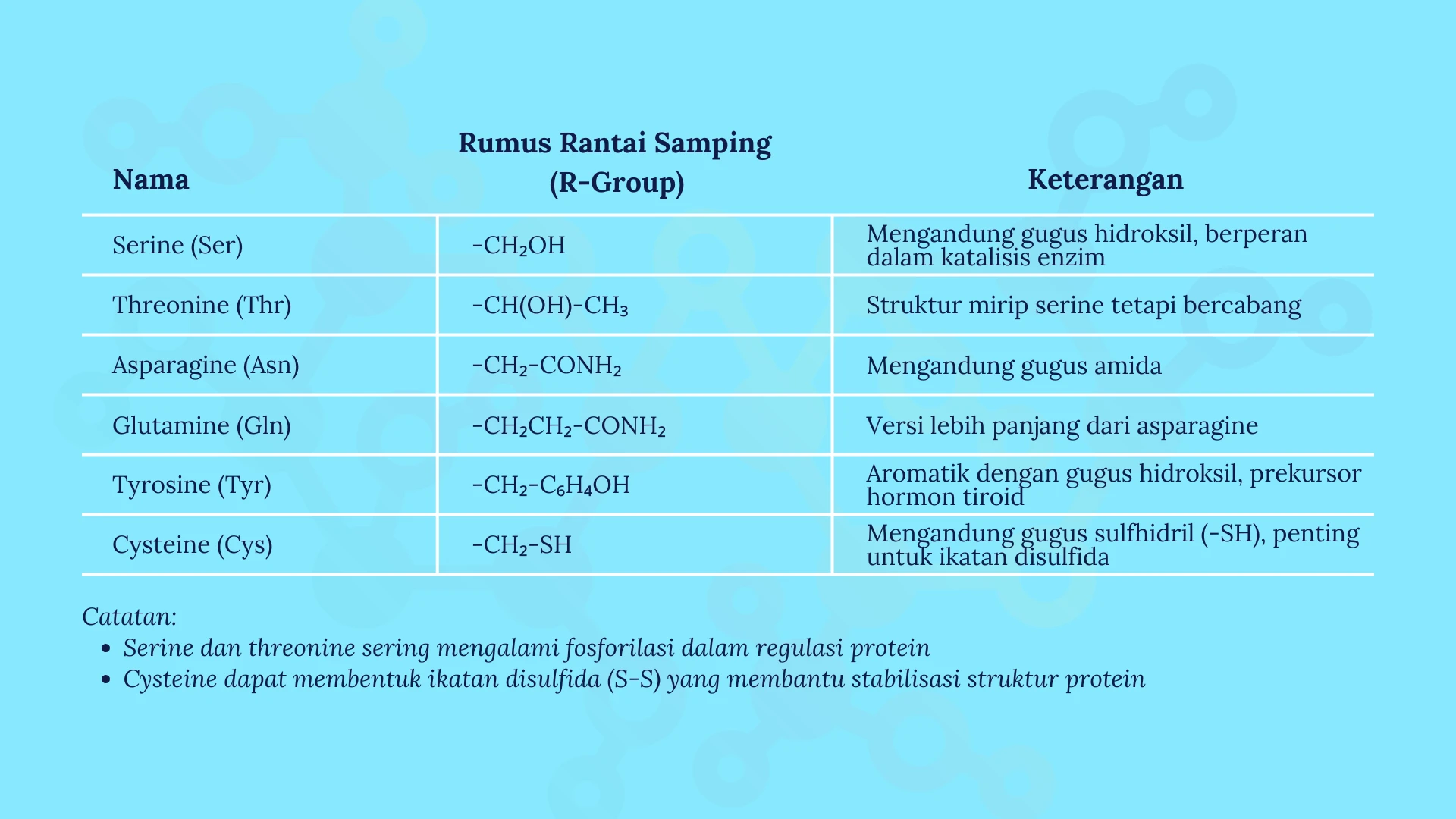
2. Asam Amino Polar Tidak Bermuatan
Asam amino dalam kelompok ini memiliki rantai samping polar, tetapi tidak memiliki muatan bersih pada pH fisiologis (~7,4). Mereka dapat membentuk ikatan hidrogen dengan air atau molekul lain, menjadikannya hidrofilik.
Ciri-ciri:
- Larut dalam air.
- Rantai samping mengandung gugus hidroksil (-OH), amida (-CONH₂), atau sulfur (-SH).
- Terlibat dalam interaksi hidrogen dan membentuk jembatan disulfida.
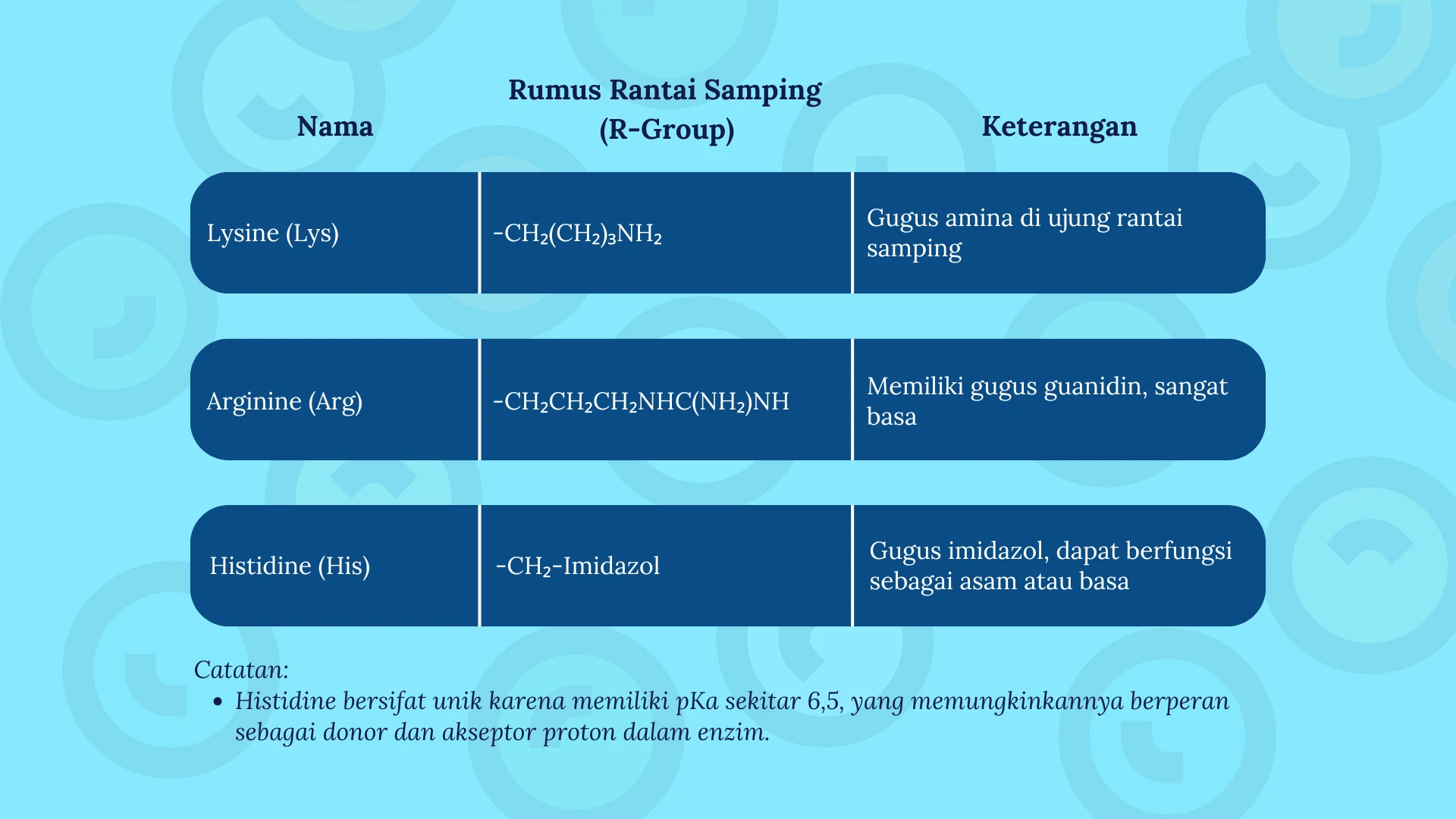
3. Asam Amino Bermuatan Positif (Basa)
Kelompok ini memiliki rantai samping basa, yang berarti mereka dapat menerima proton (H⁺) dan menjadi bermuatan positif pada pH fisiologis.
Ciri-ciri:
- Larut dalam air.
- Sering ditemukan dalam sisi aktif enzim atau protein interaksi DNA.
- Memiliki peran dalam ikatan elektrostatik.
4. Asam Amino Bermuatan Negatif (Asam)
Asam amino dalam kategori ini memiliki rantai samping asam, yang berarti mereka dapat melepaskan proton (H⁺) dan menjadi bermuatan negatif pada pH fisiologis.
Ciri-ciri:
- Larut dalam air.
- Berperan dalam reaksi biokimia dan interaksi elektrostatik.
- Sering ditemukan dalam sisi aktif enzim.
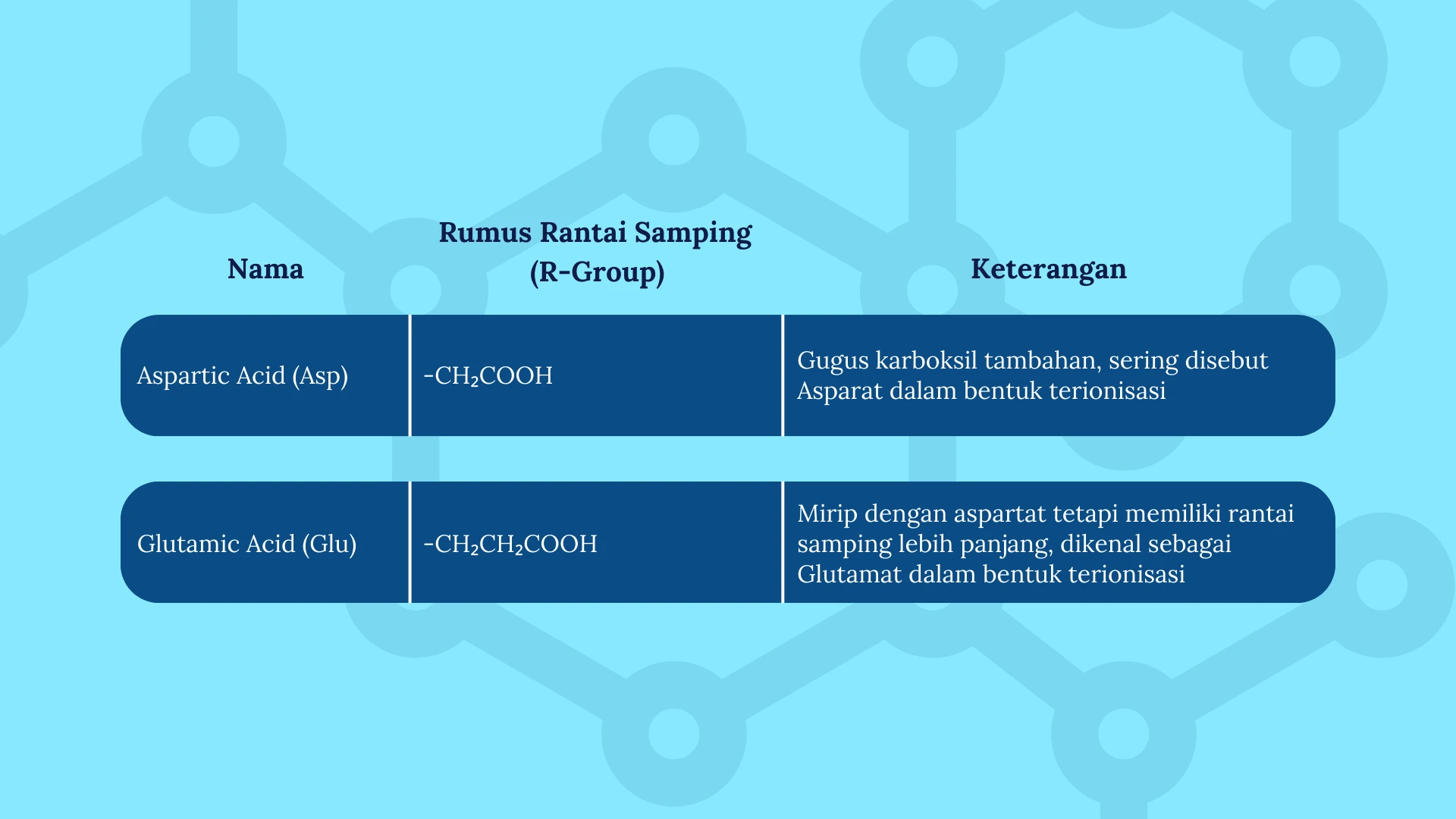
Catatan:
- Glutamat berperan dalam neurotransmisi sebagai neurotransmitter eksitatori utama di otak.
- Aspartat juga terlibat dalam siklus urea dan sintesis nukleotida
B. Berdasar Kebutuhan Nutrisi
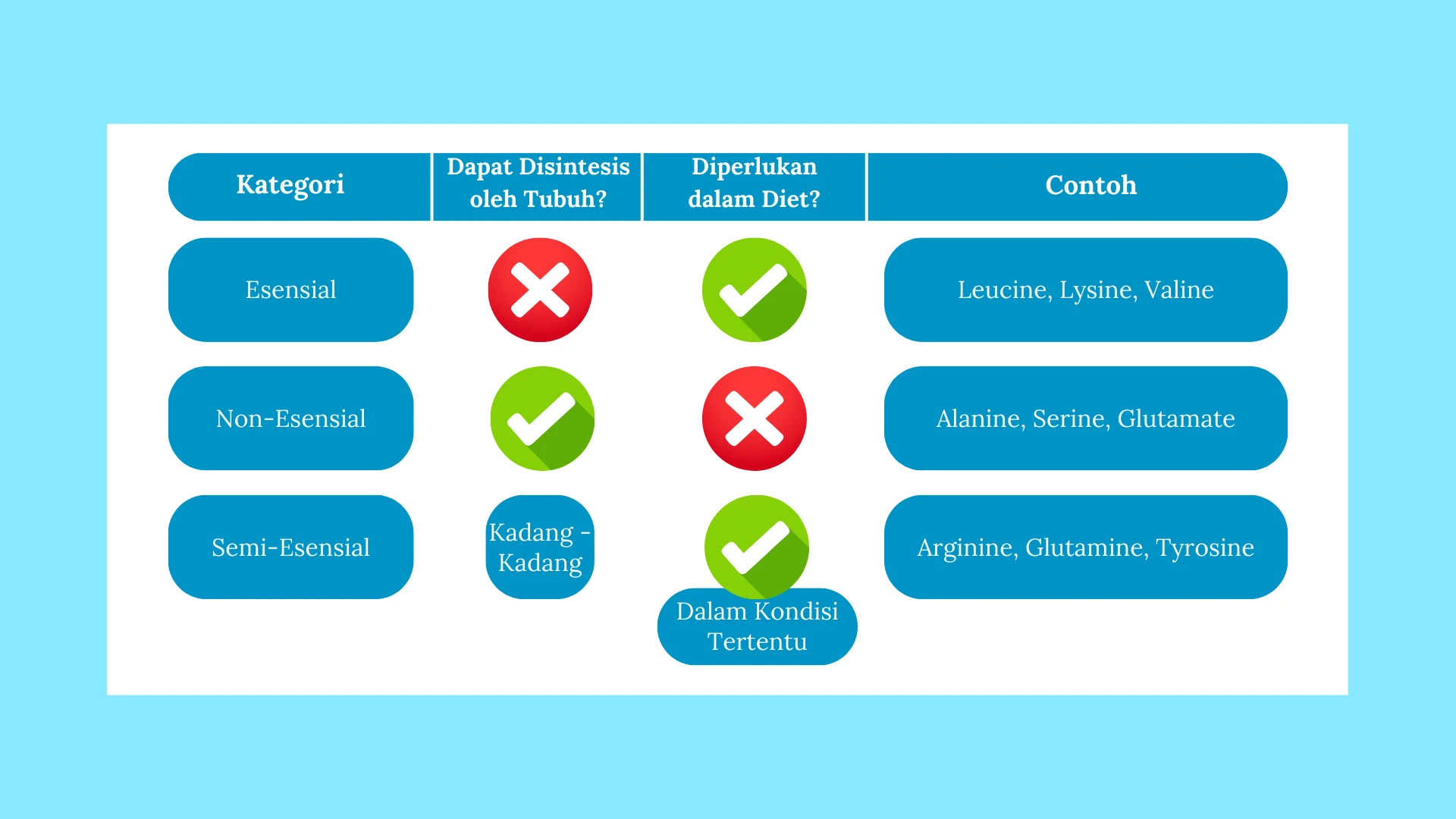
Asam amino dapat diklasifikasikan berdasarkan apakah tubuh manusia dapat memproduksinya sendiri atau tidak. Berdasarkan aspek ini, asam amino dikategorikan menjadi tiga kelompok utama:
- Asam Amino Esensial → Tidak dapat disintesis oleh tubuh, harus diperoleh dari makanan.
- Asam Amino Non-Esensial → Dapat disintesis oleh tubuh dalam jumlah cukup.
- Asam Amino Semi-Esensial (Kondisional) → Dapat disintesis oleh tubuh tetapi menjadi esensial dalam kondisi tertentu, seperti penyakit, stres fisiologis, atau pertumbuhan.
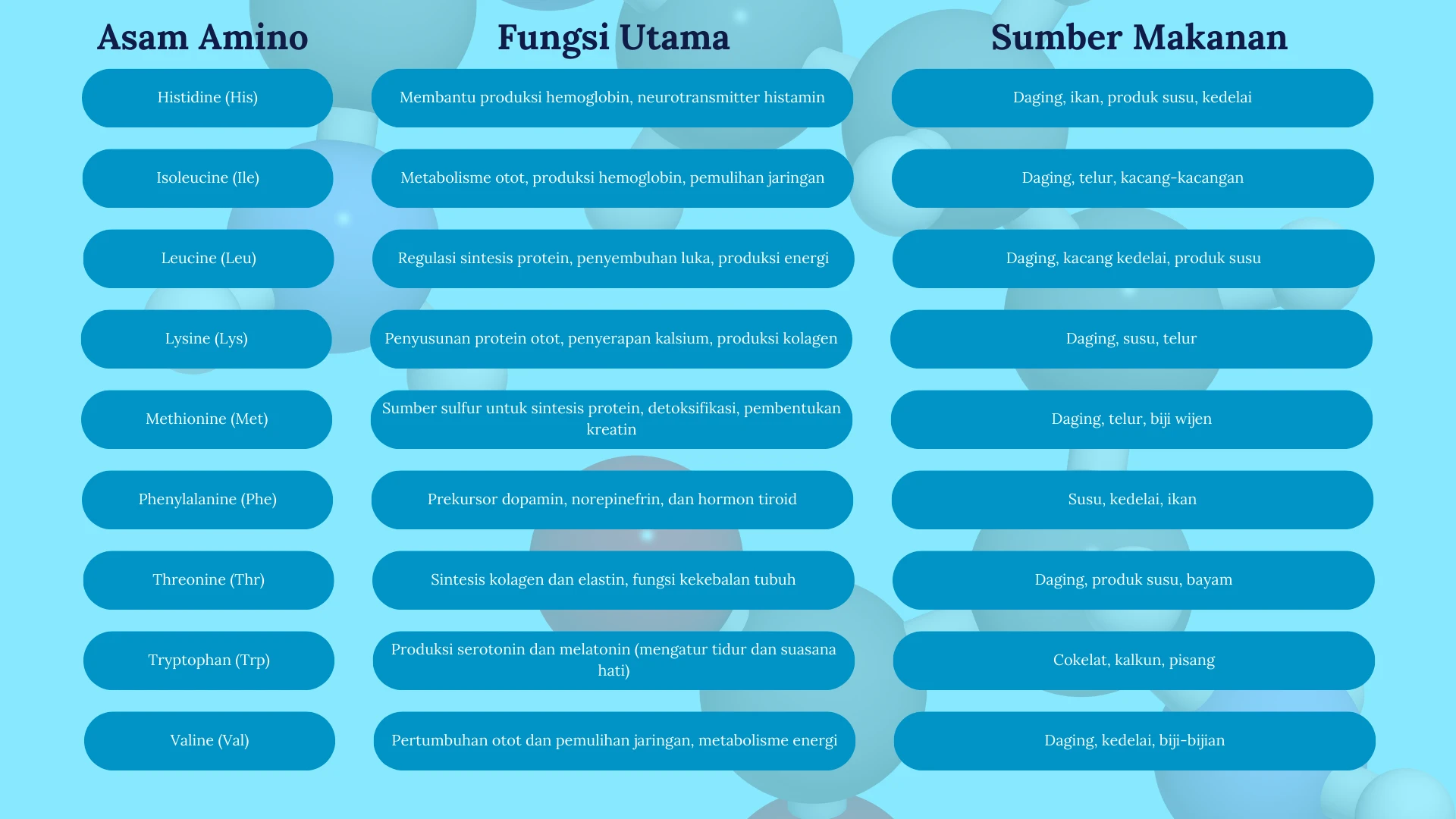
1. Asam Amino Esensial
Asam amino esensial adalah asam amino yang tidak dapat diproduksi oleh tubuh dalam jumlah yang cukup, sehingga harus diperoleh dari makanan.
Ciri-ciri:
- Harus dikonsumsi dari sumber makanan seperti daging, ikan, telur, susu, dan kacang-kacangan.
- Berperan penting dalam pertumbuhan, perbaikan jaringan, dan fungsi metabolisme.
- Kekurangan asam amino esensial dapat menyebabkan pertumbuhan terhambat, kehilangan massa otot, dan gangguan kesehatan.
2. Asam Amino Non-Esensial
Asam amino non-esensial adalah asam amino yang dapat disintesis oleh tubuh, sehingga tidak perlu diperoleh dari makanan dalam jumlah besar.
Ciri-ciri:
- Tubuh dapat memproduksinya dari asam amino lain atau senyawa metabolik.
- Tetap penting untuk fungsi biologis seperti sintesis protein, metabolisme energi, dan regulasi sistem kekebalan.

3. Asam Amino Semi-Esensial (Kondisional)
Asam amino semi-esensial adalah asam amino yang biasanya dapat disintesis oleh tubuh, tetapi dalam kondisi tertentu, tubuh tidak dapat memproduksinya dalam jumlah yang cukup.
Kondisi di Mana Asam Amino Ini Menjadi Esensial:
- Pertumbuhan cepat (misalnya pada anak-anak, bayi prematur).
- Stres fisiologis (seperti trauma, operasi, atau infeksi).
- Gangguan metabolisme tertentu.
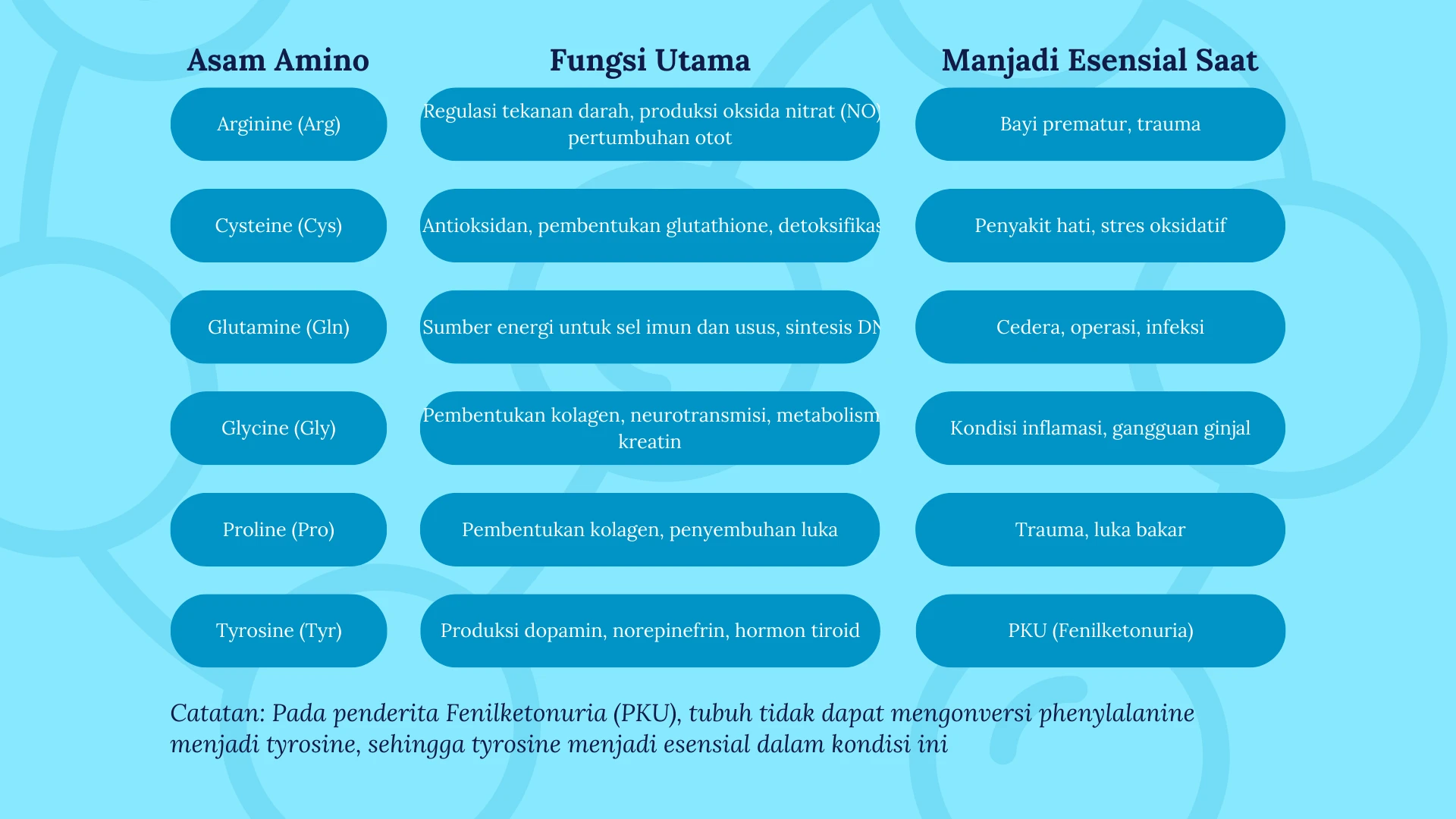
Asam amino esensial tidak dapat diproduksi oleh tubuh dan harus diperoleh dari makanan, seperti histidine, lysine, methionine, dan valine. Asam amino non-esensial dapat diproduksi oleh tubuh dari senyawa metabolik lain dan tidak harus diperoleh dari diet, seperti alanine, asparagine, dan glutamate. Asam amino semi-esensial hanya menjadi esensial dalam kondisi tertentu, seperti arginine dan glutamine, yang dibutuhkan lebih banyak saat tubuh mengalami stres atau trauma.
Sumber makanan lengkap seperti daging, ikan, telur, susu, dan kacang-kacangan sangat penting untuk mendapatkan spektrum lengkap asam amino esensial. Penting bagi atlet dan pasien tertentu untuk mendapatkan suplemen BCAA (leucine, isoleucine, valine) untuk meningkatkan pemulihan otot dan energi. Dengan memahami klasifikasi ini, kita dapat mengoptimalkan pola makan dan memastikan tubuh mendapatkan semua asam amino yang dibutuhkan untuk kesehatan dan kinerja optimal.
3.Fungsi Biologis Asam Amino
1. Penyusun Protein dan Enzim
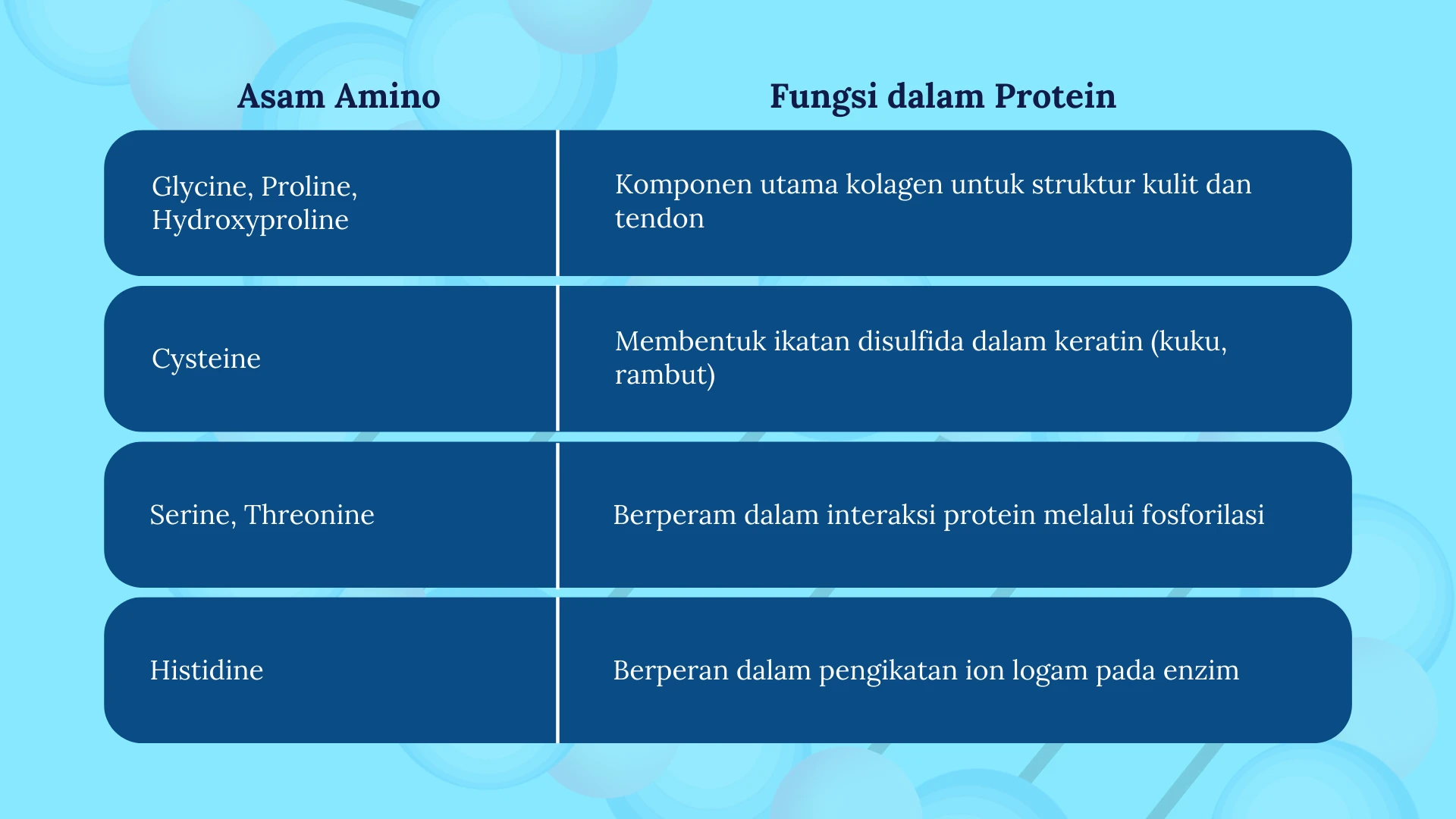
- Asam amino adalah unit dasar penyusun protein yang membentuk enzim, antibodi, hormon, dan protein struktural seperti kolagen, keratin, dan elastin.
- Enzim yang terdiri dari asam amino bertindak sebagai biokatalis, mempercepat reaksi biokimia dalam tubuh.
- Protein yang tersusun dari asam amino berperan dalam pertumbuhan, regenerasi sel, dan pemeliharaan jaringan tubuh.
2. Sumber Energi (Glukoneogenesis & Ketogenesis)
- Dalam kondisi defisit energi atau puasa, beberapa asam amino dapat diubah menjadi glukosa (glukoneogenesis) atau badan keton (ketogenesis) untuk digunakan sebagai sumber energi.
- Alanine dan glutamine sering digunakan untuk menghasilkan glukosa di hati.
- Leucine dan lysine dapat diubah menjadi badan keton untuk digunakan sebagai energi alternatif bagi otak dan otot.
Jenis Asam Amino Berdasarkan Produksi Energinya
- Asam Amino Glukogenik → Dapat diubah menjadi glukosa melalui glukoneogenesis.
- Contoh: Alanine, Aspartate, Glutamate.
- Asam Amino Ketogenik → Dapat diubah menjadi badan keton sebagai sumber energi alternatif.
- Contoh: Leucine, Lysine.
- Asam Amino Glukogenik & Ketogenik → Bisa menghasilkan glukosa dan badan keton.
- Contoh: Isoleucine, Phenylalanine, Tyrosine.
Contoh: Saat puasa atau olahraga intensif, alanine dan glutamine akan dikonversi menjadi glukosa di hati.
3. Prekursor Neurotransmitter dan Hormon
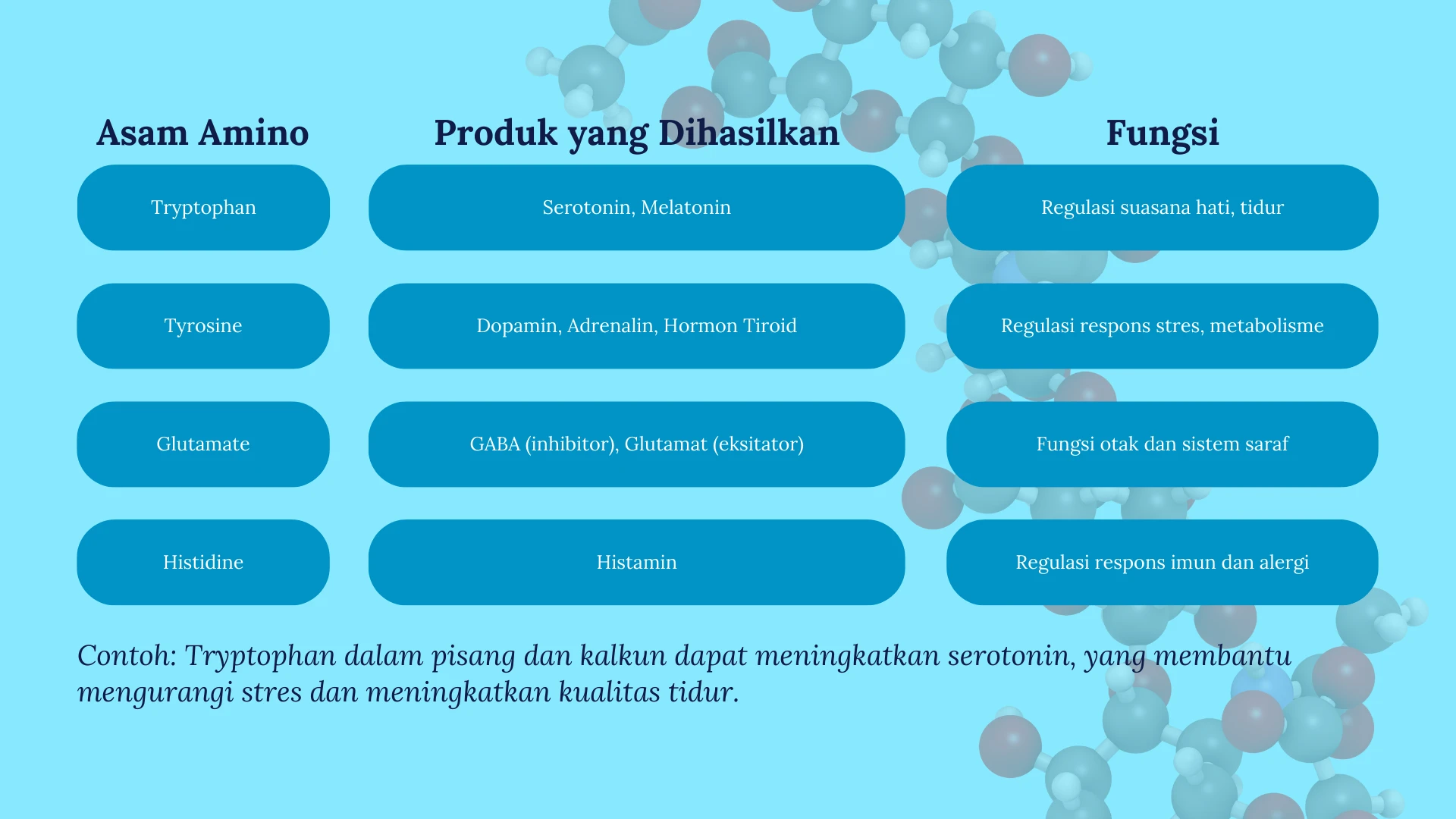
Beberapa asam amino digunakan untuk sintesis neurotransmitter dan hormon yang mengatur sistem saraf dan metabolisme:
- Tryptophan → Serotonin (pengatur suasana hati) dan Melatonin (pengatur tidur).
- Tyrosine → Dopamin, Adrenalin, dan Norepinefrin (mengontrol stres dan motivasi).
- Histidine → Histamin (terlibat dalam respons imun dan regulasi lambung).
- Glutamate → Glutamat (neurotransmitter eksitatori utama) dan GABA (neurotransmitter inhibitor).
4. Regulasi pH sebagai Buffer Biologis
- Histidine → Bertindak sebagai buffer dalam hemoglobin, membantu mempertahankan pH darah sekitar 7,35-7,45.
- Glutamate dan Aspartate → Berperan dalam regulasi pH sel melalui transport ion.
- Berperan dalam sistem buffer biologis untuk mencegah asidosis atau alkalosis yang dapat mengganggu fungsi sel.
Contoh: Saat terjadi asidosis (pH darah turun), asparagin dan glutamin membantu menyeimbangkan pH dengan mengeluarkan amonia.
5. Transportasi dan Penyimpanan Nutrisi
- Glutamine → Mengangkut nitrogen dalam darah untuk sintesis protein dan detoksifikasi amonia.
- Arginine → Membantu sintesis oksida nitrat (NO) yang meningkatkan aliran darah dan memperlebar pembuluh darah.
- Cysteine → Membantu pembentukan glutathione, antioksidan utama tubuh yang melindungi sel dari kerusakan oksidatif.
6. Sintesis DNA dan RNA
- Beberapa asam amino berperan dalam sintesis nukleotida yang membentuk DNA dan RNA:
- Aspartate dan glutamine → Prekursor dalam sintesis pirimidin (C, T, U) dan purin (A, G).
- Glycine → Membantu pembentukan cincin purin.
- Tanpa pasokan asam amino yang cukup, sintesis DNA akan terganggu, memperlambat pertumbuhan dan regenerasi sel.
7. Detoksifikasi dan Metabolisme Limbah
- Siklus Urea → Asam amino membantu mengubah amonia beracun menjadi urea, yang kemudian dikeluarkan melalui urin.
- Arginine dan ornithine berperan dalam proses detoksifikasi nitrogen untuk mencegah keracunan amonia dalam tubuh.
- Glutamine dan Aspartate → Berperan dalam pengangkutan nitrogen untuk pembuangan limbah metabolik.
8. Fungsi Imun dan Antioksidan
- Cysteine → Prekursor utama glutathione, antioksidan yang melindungi sel dari stres oksidatif.
- Glutamine → Sumber energi utama bagi limfosit dan makrofag, yang membantu tubuh melawan infeksi.
- Arginine → Meningkatkan produksi sel imun dan mempercepat penyembuhan luka.
9. Regulasi Metabolisme dan Fungsi Otot
- Branched-Chain Amino Acids (BCAA):
- Leucine → Merangsang sintesis protein otot dan pemulihan jaringan.
- Isoleucine → Mengatur metabolisme energi dan meningkatkan daya tahan otot.
- Valine → Mencegah kerusakan otot akibat latihan intens.
- Arginine → Meningkatkan aliran darah ke otot untuk mendukung pertumbuhan dan pemulihan otot.

4.Sifat Optis asam amino
Sifat optis asam amino berkaitan dengan bagaimana molekul asam amino membelokkan cahaya terpolarisasi akibat adanya pusat kiral dalam strukturnya. Sifat ini sangat penting dalam biokimia, farmasi, dan sintesis protein, karena mempengaruhi bagaimana asam amino berinteraksi dengan enzim dan biomolekul lainnya.
1. Pengertian Sifat Optis dalam Asam Amino
Sifat optis mengacu pada kemampuan suatu molekul untuk membelokkan cahaya terpolarisasi saat cahaya melewati larutannya. Hal ini terjadi karena sebagian besar asam amino memiliki atom karbon kiral (Cα), yang menyebabkan molekul tersebut memiliki dua isomer enansiomer: L-asam amino dan D-asam amino.
Catatan: Cahaya terpolarisasi adalah cahaya yang getarannya hanya terjadi dalam satu bidang tertentu.
2. Kiralitas dalam Asam Amino
A. Atom Karbon Kiral (Cα)
- Sebagian besar asam amino (kecuali glisin) memiliki atom karbon alfa kiral yang mengikat empat gugus yang berbeda:
- Gugus amina (-NH₂)
- Gugus karboksil (-COOH)
- Rantai samping (R-group)
- Atom hidrogen (-H)
- Karena memiliki empat gugus berbeda, karbon alfa ini asimetris, yang menghasilkan dua bentuk enansiomer dengan sifat optis berbeda.
B. Enansiomer L dan D
Asam amino dapat terbentuk dalam dua konfigurasi yang merupakan bayangan cermin satu sama lain, yaitu:
- L-Asam Amino (Levorotatory / "Left")
- Umum dalam protein biologis yang digunakan oleh organisme hidup.
- Digunakan dalam sintesis protein melalui ribosom.
- Contoh: L-Alanine, L-Leucine, L-Tryptophan.
- D-Asam Amino (Dextrorotatory / "Right")
- Jarang ditemukan dalam organisme eukariotik.
- Sering ditemukan dalam dinding sel bakteri dan beberapa peptida antibiotik.
- Contoh: D-Alanine, D-Glutamate dalam dinding sel bakteri.
Fakta Biologis: Hampir semua protein dalam organisme hidup tersusun dari L-asam amino, karena sistem biologis telah berevolusi untuk mengenali dan menggunakan bentuk ini secara spesifik.
3. Efek Sifat Optis pada Pembelokan Cahaya
Ketika larutan asam amino dikenai cahaya terpolarisasi, enansiomer berbeda akan membelokkan cahaya dalam arah yang berbeda:
- Enansiomer L (-) → Membelokkan cahaya ke kiri (Levorotasi)
- Enansiomer D (+) → Membelokkan cahaya ke kanan (Dextrorotasi)
Pembelokan ini dapat diukur menggunakan polarimeter, dan besarnya sudut putaran disebut sudut rotasi spesifik ([α]).
Contoh:
- L-Alanine memiliki sudut rotasi negatif (-).
- D-Alanine memiliki sudut rotasi positif (+).
Namun, perlu dicatat bahwa konfigurasi L dan D tidak selalu berhubungan langsung dengan arah putaran cahaya. Sebuah L-asam amino bisa saja memiliki rotasi cahaya ke kanan atau ke kiri, tergantung pada strukturnya.
4. Konvensi Fischer dan Penamaan L/D
Sistem konfigurasi L/D pada asam amino ditentukan berdasarkan hubungan dengan D-Gliseraldehida dalam sistem proyeksi Fischer:
- Jika gugus amina (-NH₂) berada di sebelah kiri dalam proyeksi Fischer, maka itu adalah L-Asam Amino.
- Jika gugus amina (-NH₂) berada di sebelah kanan, maka itu adalah D-Asam Amino.
Konfigurasi L/D ini tidak selalu berkaitan dengan rotasi cahaya (levorotasi/dextrorotasi), karena pengaruh rantai samping (R-group) dapat mengubah arah putaran.
5. Peran Biologis Sifat Optis Asam Amino
Sifat optis asam amino sangat penting dalam interaksi enzim dan sintesis protein:
- Hanya L-Asam Amino yang digunakan dalam protein biologis
- Ribosom mengenali L-asam amino, bukan D-asam amino.
- Protein dengan struktur tiga dimensi yang spesifik hanya bisa terbentuk jika menggunakan isomer L.
- D-Asam Amino dalam Bakteri dan Peptida Antibiotik
- D-Alanine dan D-Glutamate ditemukan dalam dinding sel bakteri untuk mencegah degradasi enzimatik oleh protease manusia.
- Beberapa antibiotik (seperti Gramicidin dan Actinomycin D) mengandung D-Asam Amino.
- Diferensiasi Enansiomer dalam Farmasi
- Banyak obat-obatan berbasis asam amino yang hanya aktif dalam satu konfigurasi optis tertentu.
- Contoh: L-DOPA (Levodopa) digunakan untuk pengobatan Parkinson, tetapi bentuk D-DOPA tidak memiliki efek yang sama.
6. Metode Penentuan Sifat Optis Asam Amino
Ada beberapa metode untuk menentukan sifat optis asam amino:
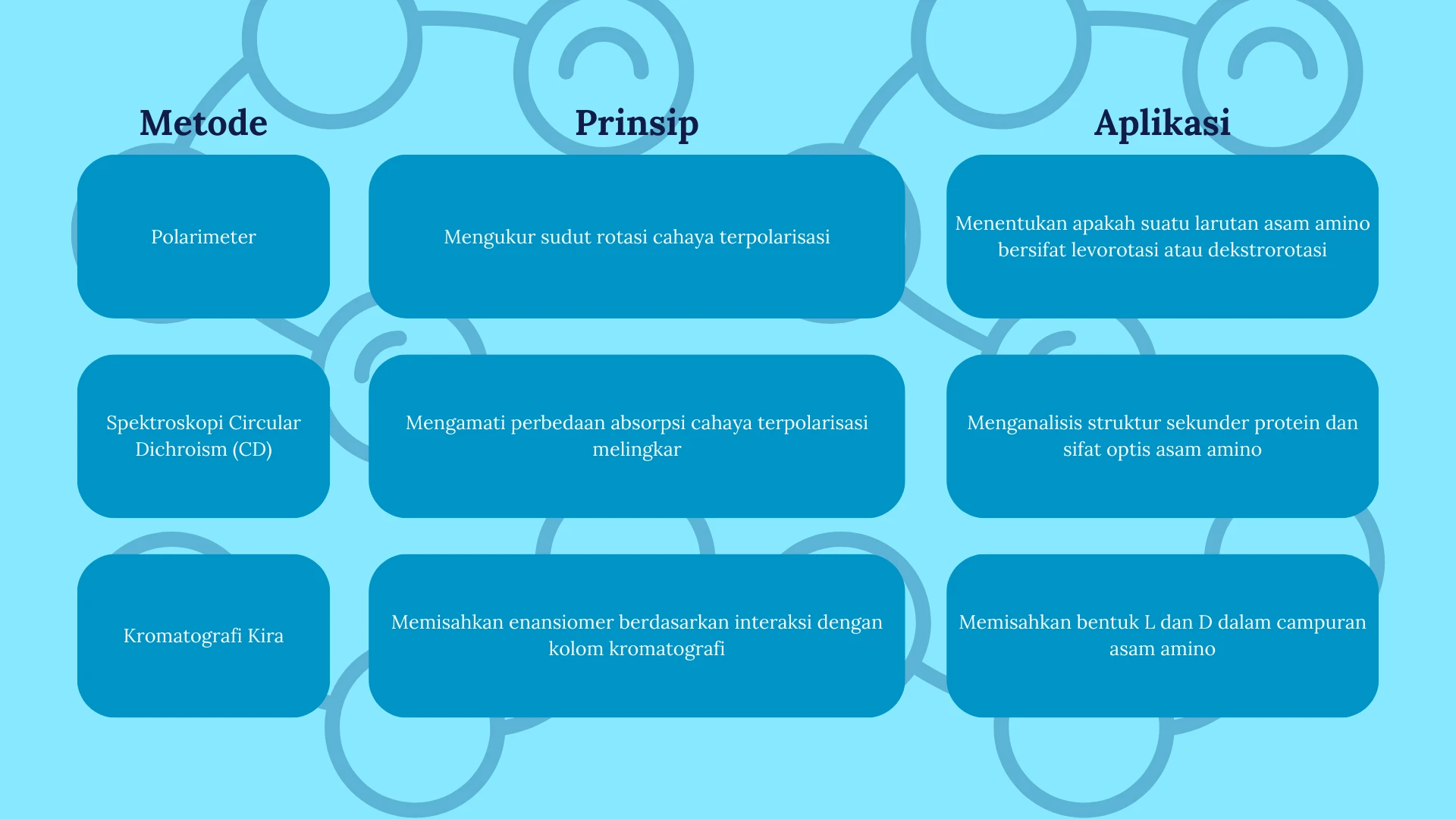
7. Perbandingan L-Asam Amino dan D-Asam Amino
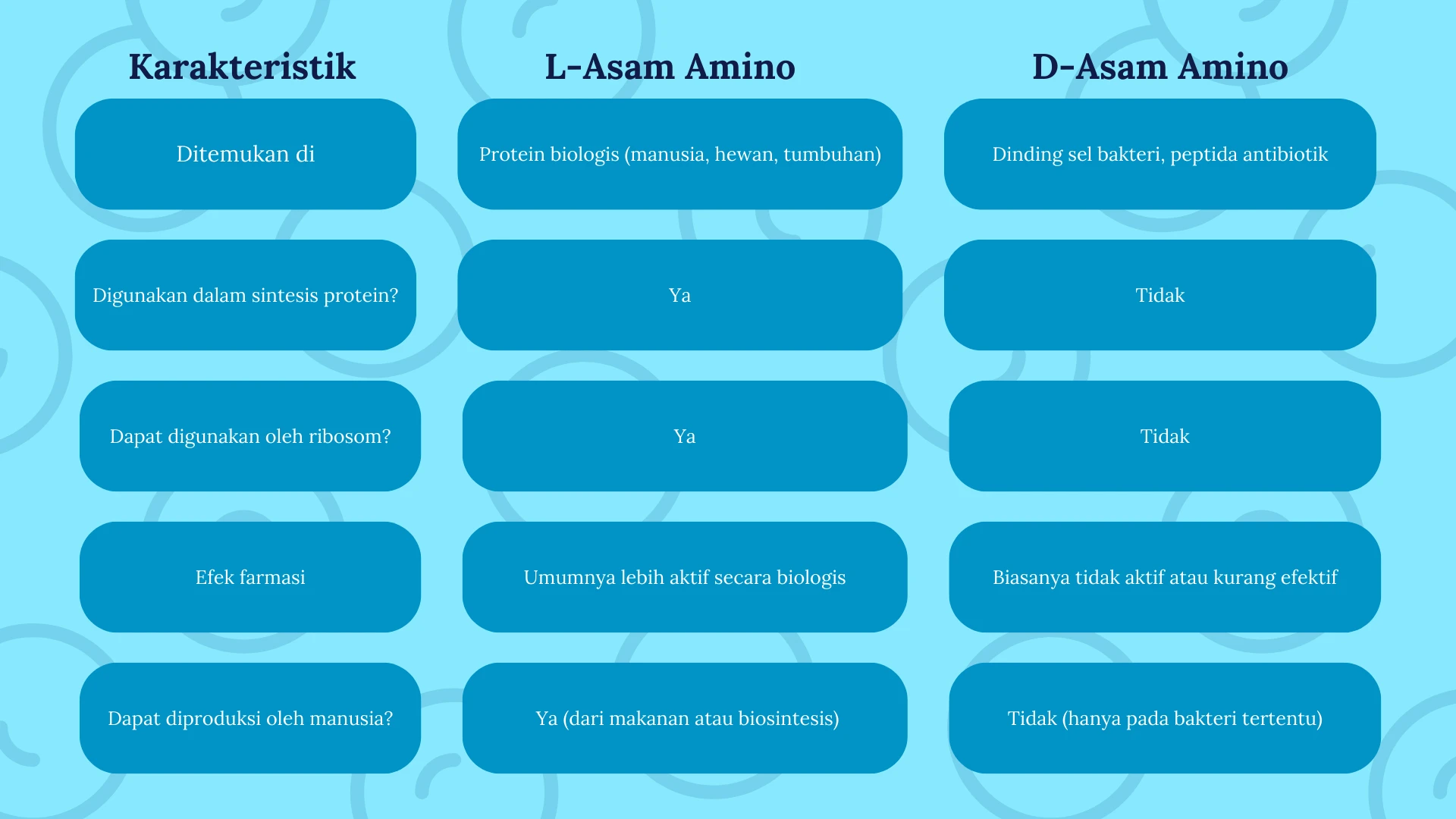
5.Reaksi Kimia Asam Amino
Asam amino memiliki berbagai reaksi kimia yang penting dalam biokimia, metabolisme, dan sintesis protein. Reaksi ini melibatkan gugus amina (-NH₂), gugus karboksil (-COOH), dan rantai samping (R-group), yang memungkinkan asam amino berperan dalam berbagai proses biologis.
1. Reaksi Pembentukan Ikatan Peptida (Kondensasi Peptida)
Penjelasan:
- Asam amino bergabung membentuk dipeptida, oligopeptida, atau polipeptida (protein) melalui ikatan peptida.
- Ikatan peptida terbentuk melalui reaksi kondensasi, yaitu pelepasan molekul air (H₂O).
Reaksi:

2. Reaksi Hidrolisis Ikatan Peptida
Penjelasan:
- Kebalikan dari reaksi kondensasi: pemecahan protein menjadi asam amino oleh hidrolisis.
- Terjadi di dalam lambung dan usus, dibantu oleh enzim protease (misalnya pepsin, trypsin, dan chymotrypsin).

3. Reaksi Dekarboksilasi Asam Amino
Penjelasan:
- Dekarboksilasi adalah penghilangan gugus karboksil (-COOH) dari asam amino untuk membentuk amina biogenik.
- Berperan dalam sintesis neurotransmitter dan hormon.

4. Reaksi Transaminasi (Pemindahan Gugus Amina)
Penjelasan:
- Transaminasi adalah pemindahan gugus amina (-NH₂) dari satu asam amino ke asam α-ketoglutarat untuk membentuk asam amino baru dan asam keto.
- Proses ini penting dalam metabolisme nitrogen dan sintesis asam amino non-esensial.

5. Reaksi Deaminasi Oksidatif (Penghilangan Gugus Amina)
Penjelasan:
- Menghilangkan gugus amina (-NH₂) dari asam amino, menghasilkan asam keto dan amonia (NH₃).
- Berperan dalam siklus urea untuk membuang kelebihan nitrogen.

6. Reaksi Oksidasi Asam Amino
Penjelasan:
- Asam amino dapat mengalami oksidasi dalam kondisi tertentu untuk menghasilkan energi atau metabolit lain.
- Reaksi ini biasanya terjadi dalam mitokondria hati.

7. Reaksi Sulfurisasi (Pembentukan Ikatan Disulfida)
Penjelasan:
- Asam amino yang mengandung sulfur (Cysteine) dapat membentuk ikatan disulfida (-S-S-).
- Ikatan ini penting dalam stabilisasi struktur protein.

- Ikatan Peptida → Membentuk protein melalui reaksi kondensasi.
- Hidrolisis Peptida → Pemecahan protein oleh enzim protease.
- Dekarboksilasi → Menghasilkan neurotransmitter seperti serotonin dan histamin.
- Transaminasi → Mengubah satu asam amino menjadi asam amino lain.
- Deaminasi Oksidatif → Membuang nitrogen dalam siklus urea.
- Oksidasi Asam Amino → Menghasilkan metabolit penting seperti tirosin dan dopamin.
- Sulfurisasi → Membentuk ikatan disulfida dalam protein struktural.
Reaksi-reaksi ini sangat penting dalam metabolisme, sintesis protein, dan detoksifikasi, yang memungkinkan tubuh menjalankan berbagai fungsi fisiologis secara optimal.
6.Siklus metabolisme asam amino
Asam amino mengalami berbagai jalur metabolisme dalam tubuh yang berperan dalam produksi energi, sintesis biomolekul penting, dan detoksifikasi nitrogen. Proses metabolisme ini mencakup degradasi asam amino, transaminasi, deaminasi, siklus urea, serta biosintesis asam amino non-esensial.
1. Jalur Utama dalam Metabolisme Asam Amino
Metabolisme asam amino dapat dikategorikan menjadi dua proses utama:
- Katabolisme (Pemecahan Asam Amino) → Menghasilkan energi atau bahan baku untuk sintesis molekul lain.
- Anabolisme (Sintesis Asam Amino dan Protein) → Menggunakan asam amino untuk membangun protein dan senyawa lain.
Berikut adalah siklus utama dalam metabolisme asam amino:
2. Katabolisme Asam Amino (Pemecahan Asam Amino)
Ketika tubuh memiliki kelebihan asam amino atau saat tubuh membutuhkan energi dalam kondisi puasa atau stres, asam amino akan dipecah menjadi produk yang bisa dimanfaatkan untuk metabolisme.
A. Reaksi Transaminasi (Pemindahan Gugus Amina)
- Fungsi: Mengubah asam amino menjadi asam keto dan membentuk asam amino baru.
- Enzim utama: Aminotransferase / Transaminase.
- Kofaktor: Vitamin B6 (Pyridoxal Phosphate, PLP).

B. Reaksi Deaminasi Oksidatif (Pelepasan Gugus Amina)
- Fungsi: Menghilangkan gugus amina (-NH₂) dari asam amino untuk menghasilkan asam keto dan amonia (NH₃).
- Lokasi: Terjadi di hati.
- Enzim utama: Glutamat Dehidrogenase.

C. Siklus Urea (Pembuangan Amonia)
- Fungsi: Membuang amonia (NH₃) yang toksik dari tubuh dengan mengubahnya menjadi urea.
- Lokasi: Terjadi di hati, dan urea kemudian diekskresikan melalui ginjal dalam urin.
Tahapan Siklus Urea:
- Amonia (NH₃) bergabung dengan CO₂ → Membentuk Karbamoil Fosfat.
- Karbamoil Fosfat + Ornithine → Citrulline (masuk ke mitokondria).
- Citrulline + Aspartate → Argininosuccinate.
- Argininosuccinate dipecah → Arginine + Fumarate.
- Arginine → Ornithine + Urea → Urea dikeluarkan melalui urin.

D. Konversi Asam Amino menjadi Energi
Asam amino dapat dikonversi menjadi dua jenis metabolit energi:
- Asam Amino Glukogenik → Dapat diubah menjadi glukosa melalui glukoneogenesis.
- Contoh: Alanine, Aspartate, Glutamate.
- Asam Amino Ketogenik → Dapat diubah menjadi badan keton untuk digunakan sebagai energi.
- Contoh: Leucine, Lysine.
- Asam Amino Glukogenik & Ketogenik → Bisa menghasilkan glukosa dan badan keton.
- Contoh: Isoleucine, Phenylalanine, Tyrosine.
3. Anabolisme Asam Amino (Sintesis Asam Amino dan Protein)
A. Sintesis Asam Amino Non-Esensial
- Asam amino non-esensial dapat disintesis dari intermediat siklus Krebs.
- Reaksi transaminasi sangat penting dalam proses ini.
Contoh Sintesis Asam Amino:
- Glutamat → Glutamin (Menggunakan ATP dan NH₃).
- Aspartat → Asparagin (Menggunakan NH₃).
- Serine → Glycine (Melalui pemindahan gugus hidroksimetil).
Catatan: Asam amino esensial tidak bisa disintesis dalam tubuh dan harus diperoleh dari makanan.
B. Sintesis Protein
- Asam amino yang sudah tersedia akan dirangkai menjadi protein dalam ribosom melalui proses translasi.
- Ikatan peptida terbentuk melalui reaksi kondensasi antara asam amino.
Tahapan Sintesis Protein:
- Transkripsi → DNA dikodekan menjadi mRNA.
- Translasi → mRNA diterjemahkan oleh ribosom untuk membentuk rantai polipeptida.
- Modifikasi Pasca-Translasi → Protein mengalami pemrosesan seperti fosforilasi, glikosilasi, atau pembentukan ikatan disulfida.
4. Hubungan Siklus Metabolisme Asam Amino dengan Jalur Metabolisme Lain
A. Hubungan dengan Siklus Krebs
- Asam keto hasil transaminasi masuk ke dalam Siklus Krebs untuk menghasilkan ATP.
- Oksaloasetat dan α-Ketoglutarat adalah intermediat utama yang terkait dengan metabolisme asam amino.
B. Hubungan dengan Glukoneogenesis
- Asam amino glukogenik dapat diubah menjadi glukosa melalui jalur glukoneogenesis di hati.
C. Hubungan dengan Lipogenesis (Pembentukan Lemak)
- Asam amino ketogenik (Leucine dan Lysine) dapat diubah menjadi badan keton atau asam lemak.
7.Pemecahan protein menjadi asam amino
Pemecahan protein menjadi asam amino adalah proses hidrolisis protein yang melibatkan enzim proteolitik dalam sistem pencernaan maupun di dalam sel. Proses ini penting untuk penyerapan nutrisi, metabolisme, serta perbaikan dan regenerasi jaringan.
1. Pengertian Pemecahan Protein
Pemecahan protein merupakan degradasi rantai polipeptida menjadi peptida kecil dan akhirnya menjadi asam amino bebas. Proses ini dilakukan oleh enzim protease atau peptidase, yang bekerja dengan cara menghidrolisis ikatan peptida yang menghubungkan asam amino dalam protein.
Pemecahan protein terjadi dalam dua skala utama:
- Ekstraseluler → Dalam sistem pencernaan untuk menyerap asam amino dari makanan.
- Intraseluler → Dalam sel untuk mendaur ulang protein yang rusak atau tidak dibutuhkan.
2. Enzim yang Berperan dalam Pemecahan Protein
Pemecahan protein menjadi asam amino bergantung pada berbagai enzim proteolitik yang bekerja di berbagai lokasi dalam tubuh. Enzim ini dibagi berdasarkan tempat kerja dan mekanisme pemecahan ikatan peptida.
A. Protease Berdasarkan Tempat Kerja
- Protease Pencernaan (Ekstraseluler)
- Diproduksi dalam lambung, pankreas, dan usus.
- Berfungsi untuk menghidrolisis protein makanan menjadi asam amino bebas.
- Protease Intraseluler
- Berperan dalam pemecahan protein yang rusak atau tidak diperlukan dalam sel.
- Terlibat dalam jalur ubiquitin-proteasome dan autofagi.
B. Protease Berdasarkan Cara Kerja
- Endopeptidase → Memecah ikatan peptida di dalam rantai polipeptida.
- Contoh: Pepsin, Trypsin, Chymotrypsin.
- Eksoprotease → Memotong asam amino satu per satu dari ujung rantai polipeptida.
- Contoh: Carboxypeptidase, Aminopeptidase.
3. Proses Pemecahan Protein dalam Sistem Pencernaan
Pemecahan protein dalam saluran pencernaan berlangsung melalui tiga tahap utama:
A. Pemecahan Protein di Lambung
- Enzim utama: Pepsin (diaktifkan dari pepsinogen oleh HCl).
- Lingkungan asam lambung (pH 1,5 – 3,5) membantu denaturasi protein, sehingga lebih mudah dipecah oleh enzim.

B. Pemecahan Protein di Usus Halus (Duodenum)
- Enzim utama: Trypsin, Chymotrypsin, Elastase (diproduksi oleh pankreas).
- Bekerja pada pH netral (~7-8).
- Mengubah polipeptida menjadi oligopeptida yang lebih kecil.

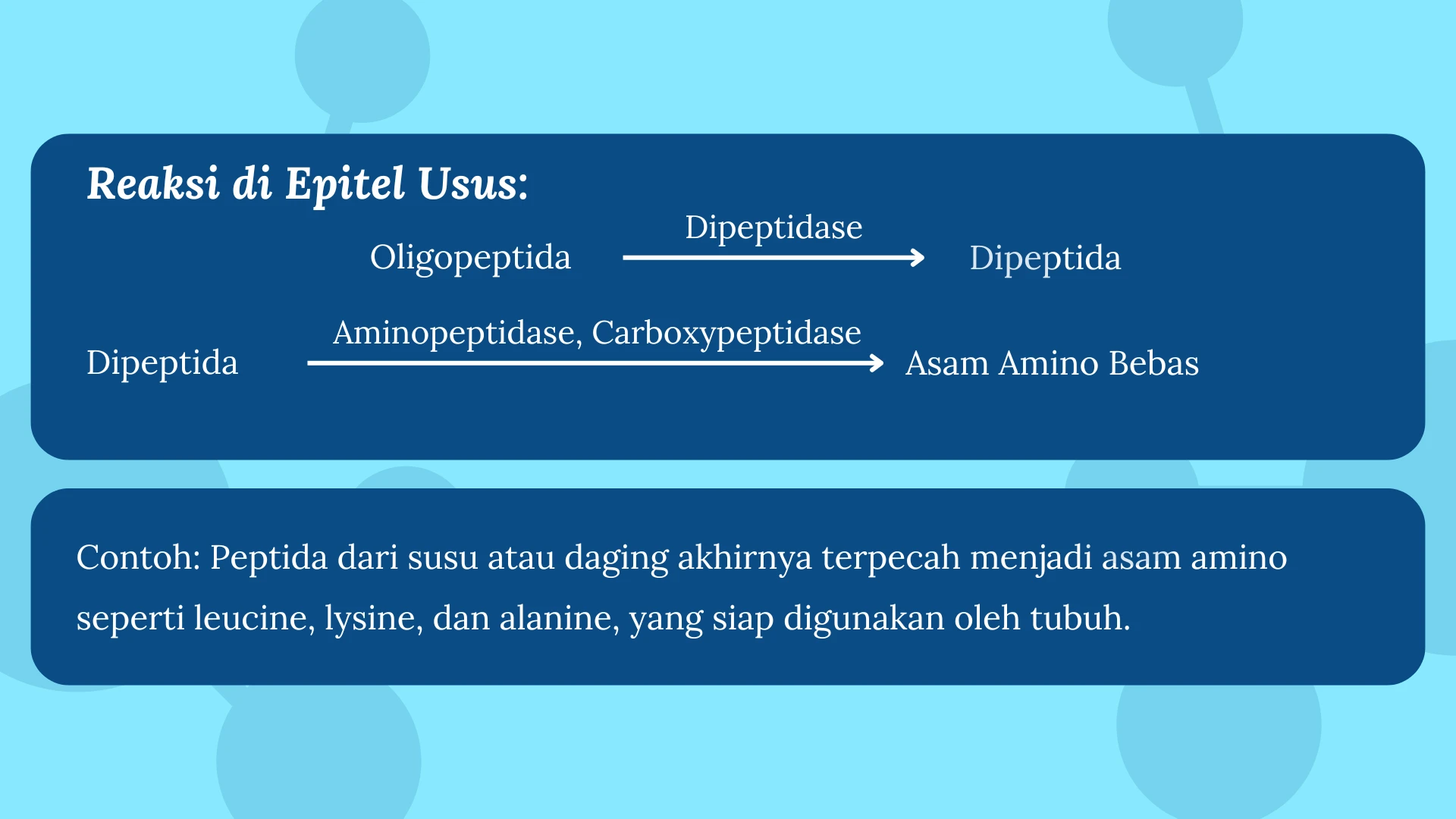
C. Pemecahan Protein di Epitel Usus
- Enzim utama: Dipeptidase, Carboxypeptidase, Aminopeptidase.
- Mengubah oligopeptida menjadi dipeptida, tripeptida, dan akhirnya asam amino bebas.
- Asam amino yang dihasilkan diserap ke dalam aliran darah melalui transport aktif dan difusi.
4. Pemecahan Protein Intraseluler (Daur Ulang Protein)
Selain pencernaan makanan, protein dalam tubuh juga mengalami pemecahan di dalam sel untuk menjaga keseimbangan protein.
A. Sistem Ubiquitin-Proteasome (Pemecahan Terarah)
- Protein yang rusak atau tidak dibutuhkan diberi tanda ubiquitin.
- Proteasome mencerna protein menjadi peptida kecil dan asam amino bebas.
- Asam amino hasil pemecahan dapat digunakan kembali untuk sintesis protein baru atau metabolisme energi.
B. Sistem Autofagi (Pembersihan Sel)
- Lisosom mencerna protein yang rusak dalam sel melalui enzim protease lisosomal.
- Terjadi saat tubuh mengalami stres seluler atau kelaparan untuk mendaur ulang protein yang ada.
5. Jalur Metabolisme Asam Amino Setelah Pemecahan Protein
Setelah protein dipecah menjadi asam amino bebas, asam amino ini dapat masuk ke berbagai jalur metabolisme:
- Sintesis Protein Baru → Digunakan untuk membangun kembali enzim, hormon, dan jaringan otot.
- Produksi Neurotransmitter → Tryptophan → Serotonin, Tyrosine → Dopamin.
- Konversi Energi → Glukoneogenesis (Glukosa) atau Ketogenesis (Badan Keton).
- Ekskresi Limbah Nitrogen → Melalui Siklus Urea di hati untuk membuang amonia.
- Perbandingan Pemecahan Protein Pencernaan vs Intraseluler

Asam amino adalah komponen fundamental dalam kehidupan, berperan sebagai penyusun utama protein serta terlibat dalam berbagai proses metabolisme dan fisiologis yang mendukung pertumbuhan, perbaikan jaringan, dan keseimbangan energi. Selain itu, asam amino juga memiliki fungsi penting dalam sintesis enzim, hormon, neurotransmitter, dan detoksifikasi nitrogen, menjadikannya elemen krusial dalam biokimia dan kesehatan manusia. Melalui proses metabolisme kompleks, asam amino dapat digunakan untuk membentuk protein baru, menghasilkan energi, atau berperan dalam komunikasi seluler. Karena peranannya yang sangat luas, asupan asam amino yang cukup dan seimbang sangat penting untuk menjaga fungsi tubuh yang optimal. Oleh karena itu, memahami struktur, fungsi, dan metabolisme asam amino tidak hanya membantu dalam ilmu kedokteran dan nutrisi, tetapi juga dalam pengembangan terapi dan teknologi bioteknologi masa depan.
